I – Tests de reconnaissance de quelques ions.
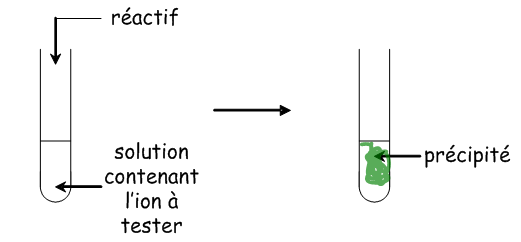
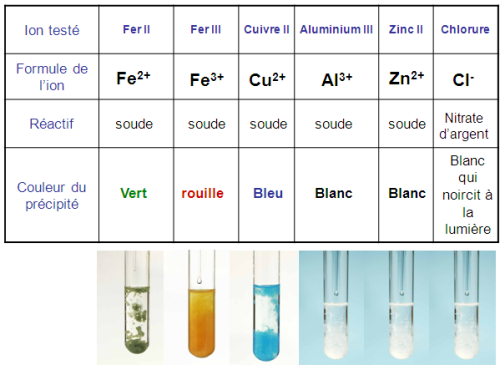
Pour mettre en évidence la présence d’ions dans des solutions, on réalise des réactions de précipitation.
Remarque : on appelle « précipité » un solide qui apparaît dans un liquide homogène. Lorsque un précipité apparaît on appelle cela une « précipitation ».
Pour réaliser les tests :
• On verse une petite quantité de solution contenant l’ion à tester dans un tube à essai.
• On rajoute ensuite quelques gouttes de réactif dans le tube à essai.
• On observe alors la couleur du précipité obtenu.
II – Mesure du pH des solutions
Le pH d’une solution aqueuse permet de savoir si une solution est acide, neutre ou basique.
Le pH d’une boisson se mesure à l’aide d’un papier indicateur de pH ou avec un appareil appelé pH-mètre.
Expérience :
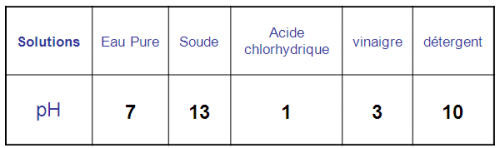
On mesure le pH de quelques solutions à l’aide du pHmètre.
On trouve les résultats suivants :
L’échelle de pH s’étale de 0 à 14.
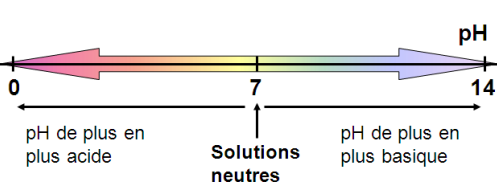
Interprétation du pH :
Toutes les solutions aqueuses contiennent des molécules d’eau, des ions hydrogène H+ et des ions hydroxyde OH–.
Une solution dont le pH est égal à 7 (neutre) contient autant d’ions H+ que d’ions OH–.
Une solution acide, comme l’acide chlorhydrique (H+, Cl–) , a un pH inférieur à 7 car elle contient davantage d’ions H+ que d’ions OH–.
Ce sont les ions H+ qui sont responsables de l’acidité.
Une solution basique, comme la soude (Na+, OH–), a un pH supérieur à 7 car elle contient davantage d’ions OH– que d’ions H+.
Ce sont les ions OH– qui sont responsables de la basicité.
Le pH de quelques produits
III – Effet de la dilution sur le pH des solutions
Expérience 1:
On dilue progressivement une solution acide avec de l’eau distillée en mesurant le pH de la solution obtenue.
Observation:
On constate que le pH de la solution augmente et se rapproche de 7. La solution devient moins acide.
Expérience 2 :
On réalise la même expérience avec une solution basique (soude).
Observation :
On constate que le pH de la solution diminue et se rapproche de 7. La solution devient moins basique.
Conclusion :
Quand on dilue une solution acide, elle devient moins acide et son pH se rapproche de 7.
Quand on dilue une solution basique, elle devient moins basique et son pH se rapproche de 7.
Les solutions acides ou basiques (certains produits ménagers) sont corrosives lorsqu ’elles sont concentrées. Il est souvent nécessaires de les diluer pour les utiliser.


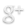






10 / 10 Tres bon cours.
Ces ce que j'apprends en cours 20/20
Cours Complet, explication simple, tout pour bien aprendre
10/10
Love that!
J espere avoir une bonne note merci
merci
Bonjour, je souhaite savoir tous les cours sont conforment avec le programme actuel
Bonjour, les cours placés dans l’onglet Cycle 4 sont conformes au programme actuel!
Ping :PH | Pearltrees
très bon cours pour apprendre merci cordialement
merci pour ce cours combien important
Love that!
Très intéressant
Merci pour ce Qcm 10/10